细胞株构建是生物制药、重组蛋白生产、基因功能研究等领域的核心底层技术,尤其在治疗性单抗、双抗、融合蛋白及重组疫苗的产业化开发中,直接决定产品的产能、质量与生产成本。近年来,随着生物药市场需求持续扩容,行业对细胞株的核心诉求愈发聚焦两大核心指标:一是高表达量,即单位细胞、单位体积内目标蛋白的产出效率,直接关联产业化产能与成本控制;二是长期稳定性,即细胞株在连续传代、大规模培养过程中,维持基因完整性、表达水平一致性及蛋白质量均一性的能力,是药品获批与规模化生产的核心前提。当前,以中国仓鼠卵巢细胞(CHO)为核心的哺乳动物细胞表达系统占据商业化主导地位,HEK293等细胞系多用于研发阶段快速表达,行业技术迭代始终围绕破解“高表达与稳定性难以兼顾”的行业痛点展开,本文重点围绕两大核心因素,梳理细胞株构建的发展现状、关键技术与现存挑战。

一、高表达量细胞株构建的核心技术与发展现状
高表达量是细胞株产业化应用的核心竞争力,早期传统细胞株构建技术多依赖随机整合与粗放筛选,表达水平仅能达到毫克级,难以满足工业化生产需求。经过数十年技术迭代,当前行业已形成从载体设计、基因整合、宿主改造到高通量筛选的全链条优化体系,重组蛋白表达量从早期不足1g/L提升至当前10-15g/L,部分优化细胞株甚至突破20g/L,核心技术突破集中在以下维度:
1. 表达载体元件的理性优化,从源头提升转录翻译效率
表达载体是调控外源基因表达的核心载体,其元件组合直接决定表达强度,当前行业已从盲目拼接转向理性设计。强启动子筛选与改造是核心环节,传统CMV启动子虽表达强度高,但易发生表观遗传沉默,目前行业多采用改造型CMV、EF1α、SV40等复合型强启动子,或适配宿主细胞的内源性启动子,兼顾转录活性与持续性;同时搭配增强子、绝缘子、基质附着区(MAR)等调控元件,破除染色质结构抑制,提升转录效率。
其次,密码子优化与翻译元件优化是关键,针对CHO等宿主细胞的密码子偏好性,对目的基因序列进行同义突变,消除稀有密码子与二级结构,大幅提升mRNA翻译效率;同时优化Kozak序列、信号肽序列,增强蛋白分泌效率,减少胞内蛋白积累导致的细胞毒性,进一步提升有效表达量。此外,双顺反子表达元件(如IRES、2A肽)的应用,实现目的基因与筛选标记的协同表达,提升阳性克隆的富集效率。
2. 基因整合策略升级,实现高效定点整合与拷贝数精准调控
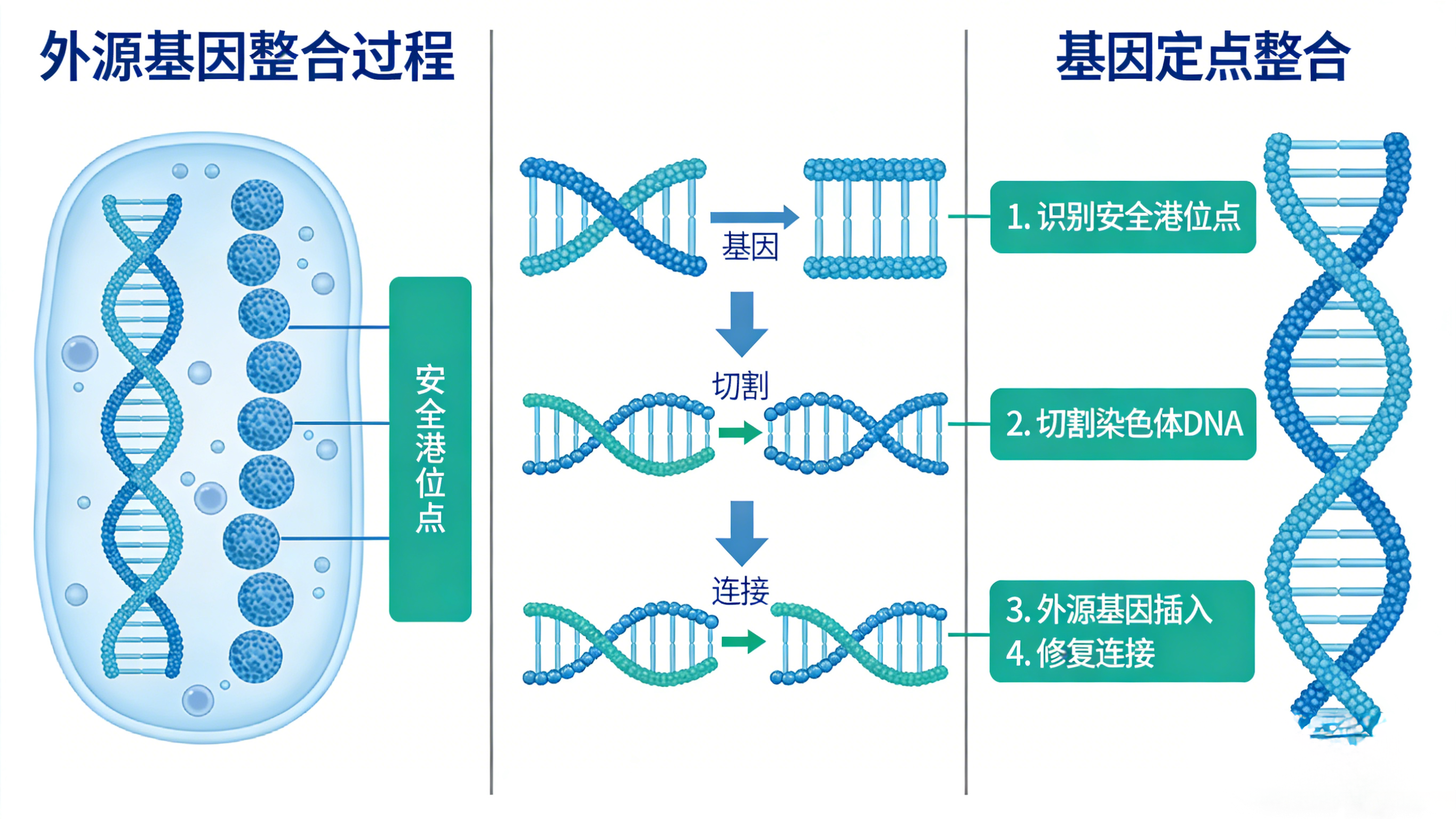
传统随机整合技术是制约表达量的核心瓶颈,外源基因随机插入宿主基因组沉默区域,不仅表达水平极低,且克隆异质性极强。当前行业逐步淘汰粗放随机整合,转向半靶向整合(STI)与位点特异性整合(SSI)技术。其中,转座子介导的半靶向整合(如PiggyBac系统)可将外源基因定向插入转录活跃区域,整合效率提升数倍,细胞池均一性大幅提高,大幅缩短筛选周期;基于CRISPR/Cas9的同源定向修复技术,实现外源基因在基因组“安全港”位点的精准单拷贝整合,彻底规避位置效应带来的表达差异,单拷贝表达效率较随机整合提升3-5倍。
同时,筛选标记系统的优化助力拷贝数精准调控,DHFR/MTX、GS/MSX筛选系统通过逐步增加筛选压力,实现外源基因拷贝数的可控扩增,既保障高表达量,又避免过度扩增导致的细胞代谢负担过重,平衡细胞生长与蛋白表达的关系。
3. 宿主细胞工程化改造,优化细胞生长与代谢特性
宿主细胞的自身生理状态直接影响表达效率,当前行业通过基因编辑技术对CHO等宿主细胞进行定向改造,提升细胞活力、抗凋亡能力与代谢效率。例如,敲除BAX/BAK等促凋亡基因,延长细胞培养周期;过表达分子伴侣蛋白,缓解内质网应激,提升蛋白正确折叠效率;优化细胞糖基化相关基因,兼顾高表达与蛋白翻译后修饰质量。同时,无血清悬浮驯化宿主细胞的普及,适配大规模生物反应器培养,进一步释放高表达潜能。
4. 高通量智能化筛选,快速富集高产克隆
传统有限稀释法筛选周期长、效率低,难以快速筛选高产克隆。当前行业普遍采用流式细胞分选(FACS)、单细胞打印、高通量孔板培养结合荧光报告基因技术,实现高表达细胞的快速富集,筛选周期从8-12周缩短至3-4周;结合人工智能与代谢组学分析,通过细胞形态、代谢参数预判表达量,进一步提升高产克隆筛选准确率,避免漏筛优质细胞株。
二、细胞株稳定性的核心影响因素与技术优化进展
稳定性是细胞株具备产业化价值的核心前提,分为遗传稳定性与表达稳定性,前者指外源基因整合位点、拷贝数在连续传代中保持稳定,后者指细胞株长期传代(通常要求60-90代)后,表达量波动控制在±15%-20%以内,且蛋白质量无明显漂移。早期高产细胞株常出现“传代后产量断崖式下跌”“基因沉默”“染色体变异”等问题,严重制约产业化应用,当前行业针对稳定性的技术优化已取得突破性进展。
1. 核心影响因素:制约稳定性的关键痛点
一是位置效应与表观遗传沉默,随机整合的外源基因易插入异染色质区域,长期培养中发生DNA甲基化、组蛋白修饰,导致转录沉默,表达量逐步衰减;二是基因拷贝数丢失,过度扩增的外源基因在细胞分裂过程中易发生片段丢失,尤其连续传代后拷贝数大幅下降,直接导致产量降低;三是宿主细胞染色体不稳定性,CHO等工程细胞本身存在染色体数目变异、易位等问题,长期悬浮培养中核型不稳定,引发细胞群体分化,高产克隆占比下降;四是细胞代谢负担失衡,高表达导致细胞代谢压力过大,生长活力衰退,间接影响表达稳定性。
2. 提升稳定性的核心技术策略
靶向基因组安全港位点整合是提升稳定性的核心手段,这类位点不干扰宿主细胞必需基因表达,染色质结构开放,能持续支持外源基因转录,彻底避免随机整合导致的表观遗传沉默。经测试,定点整合细胞株连续传代90天(26代)以上,表达量波动控制在20%以内,基因拷贝数无明显变化,远优于随机整合细胞株,已成为商业化生产细胞株的主流构建策略。
(2)载体元件优化,抵御表观遗传沉默
在表达载体中加入MAR元件、绝缘子序列,阻断周边染色质的抑制信号,维持基因转录活性;改造启动子序列,降低甲基化位点概率,选用宿主细胞内源性启动子,减少外源启动子的沉默风险。同时,采用低拷贝精准整合替代高拷贝随机扩增,避免基因片段丢失,兼顾表达量与遗传稳定性,破解“高产不稳”的行业难题。
(3)宿主细胞稳定性改造,强化遗传稳健性
通过基因编辑技术修复宿主细胞染色体缺陷,敲除异常重组相关基因,提升染色体分裂稳定性;筛选核型稳定的宿主细胞亚株,作为细胞株构建的底盘细胞,从源头降低群体分化风险。同时,优化细胞培养工艺,采用无血清化学成分明确培养基,配合动态补料策略,减轻细胞代谢负担,维持细胞生理状态稳定,间接保障表达持续性。
(4)严格的稳定性验证体系,适配产业化标准
当前行业已建立标准化稳定性验证流程,要求细胞株连续传代60代以上,定期检测基因拷贝数、mRNA表达水平、蛋白产量及质量指标,同时通过核型分析、Southern blot等技术验证遗传完整性。监管机构对生产用细胞株的稳定性要求愈发严格,稳定期不足、表达波动超标的细胞株无法获批工业化生产,倒逼技术迭代向“高产且长效稳定”方向发展。

三、当前技术瓶颈与前沿发展趋势
1. 现存核心瓶颈
尽管高表达量与稳定性技术取得显著突破,但仍存在部分行业痛点:一是定点整合技术虽稳定性优异,但部分位点表达强度仍有提升空间,且构建成本较高、工艺复杂度提升;二是特殊蛋白(如复杂糖基化蛋白、毒性蛋白)的细胞株构建,难以同时兼顾高表达、稳定性与蛋白活性;三是小规模筛选与大规模生物反应器培养的适配性差异,部分实验室高产细胞株在规模化生产中稳定性下降、表达量衰减;四是克隆异质性问题仍未完全消除,即使定点整合,仍存在少量细胞群体表达差异。
2. 前沿发展趋势
未来细胞株构建技术将朝着精准化、智能化、标准化方向发展,合成生物学与人工智能的深度融合成为核心驱动力。一方面,通过模块化载体设计、多基因协同调控,构建自适应代谢平衡的细胞株,实现高表达与稳定性的完美兼容;另一方面,AI辅助的启动子、信号肽理性设计,大幅提升元件优化效率与成功率;同时,一次性整合、无筛选标记细胞株构建技术,简化工艺流程,降低监管风险;此外,通用型底盘细胞株的开发,实现不同目标蛋白的快速适配,缩短细胞株开发周期,适配生物药快速迭代的市场需求。
细胞株构建技术已从早期的粗放随机构建,迈入精准化、理性设计的新阶段,高表达量与稳定性不再是相互矛盾的指标,而是通过载体优化、定点整合、宿主改造、智能化筛选等技术实现协同提升。当前,
CHO细胞仍是商业化生产的核心宿主,定点整合、基因编辑技术成为行业主流,细胞株表达量与稳定性指标持续突破,大幅降低生物药生产成本、提升产品质量均一性。
未来,随着技术持续迭代,细胞株构建将进一步突破现有瓶颈,实现从“高产”到“高产稳产”、从“实验室适配”到“全规模化生产适配”的升级,为创新生物药的研发与产业化提供更坚实的底层支撑,同时推动生物制药行业向高效、低成本、标准化方向持续发展。


