近日,大湾生物旗下CHO-K1目录培养基AlfaMedX K1成功获得美国食品药品监督管理局(FDA)药物主文件(DMF)备案,备案号:42995。这一成果,标志着大湾生物培养基产品在全球化布局与商业化落地进程中,继通过ISO 9001:2015认证后,再添一座重要里程碑。
依托DMF备案,AlfaMedX K1产品将为全球客户带来切实便利:客户在使用AlfaMedX K1目录培养基进行FDA新药注册申报时,可直接引用该DMF备案号,极大地缩短产品审查和评估时间,简化申报资料包,进一步加速药物项目的获批与上市进程。

▲CHO-K1目录培养基AlfaMedX K1完成FDA的DMF备案
AlfaMedX K1目录培养基是大湾生物AlfaMedX平台运用AI等前沿技术对大量试验数据分析与预测,优化了培养基的成分配比及使用条件,专门针对CHO-K1细胞株开发的目录培养基,满足增强细胞生长,提高蛋白表达等需求。
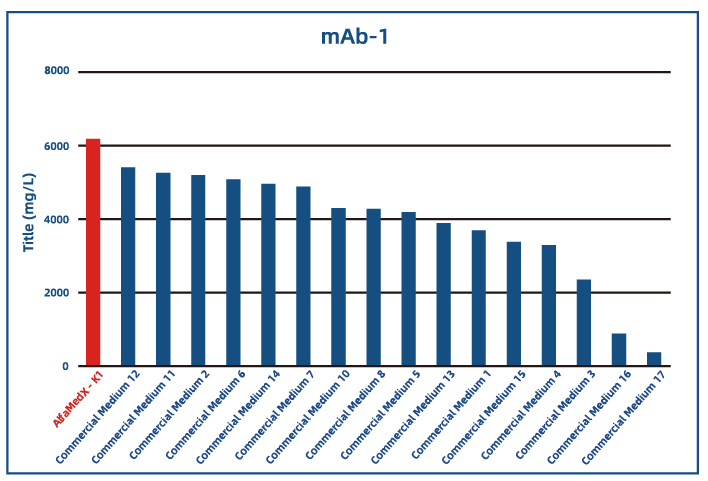
经实验数据对比,AlfaMedX K1目录培养基在CHO-K1细胞培养中,相较于市面上17家常用商业化培养基,在单抗、双抗、融合蛋白等产品的细胞株培养中,充分展现出“表达性能优异”与“适应性广”的核心优势。
● 单抗应用
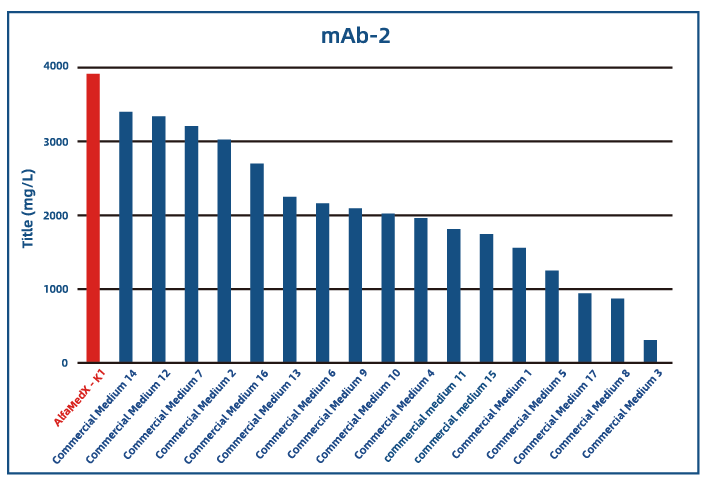
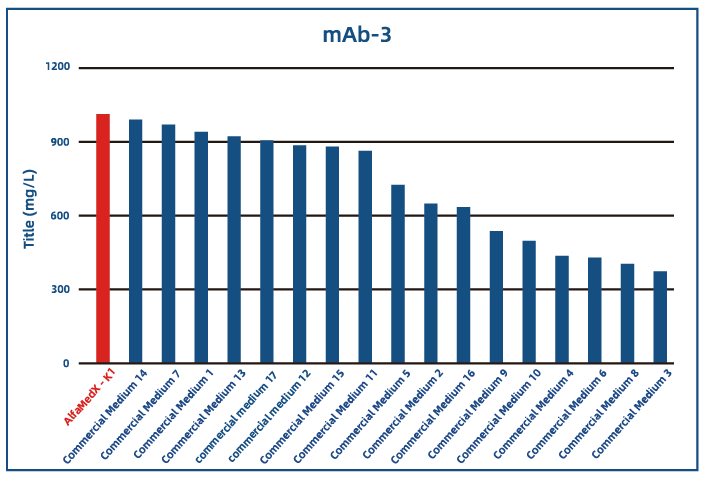
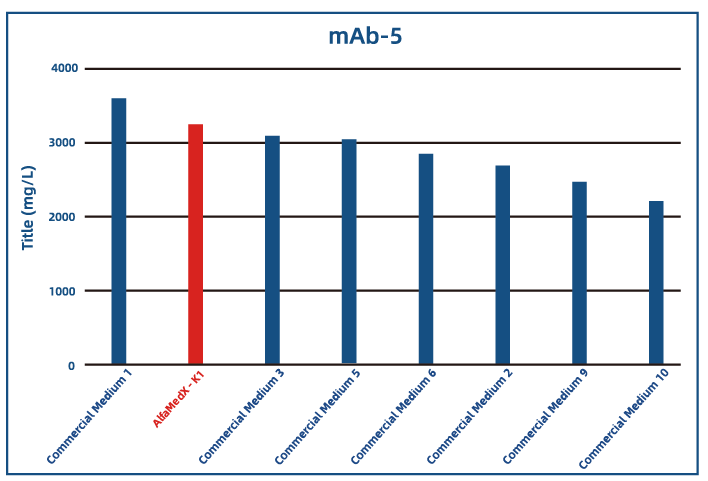
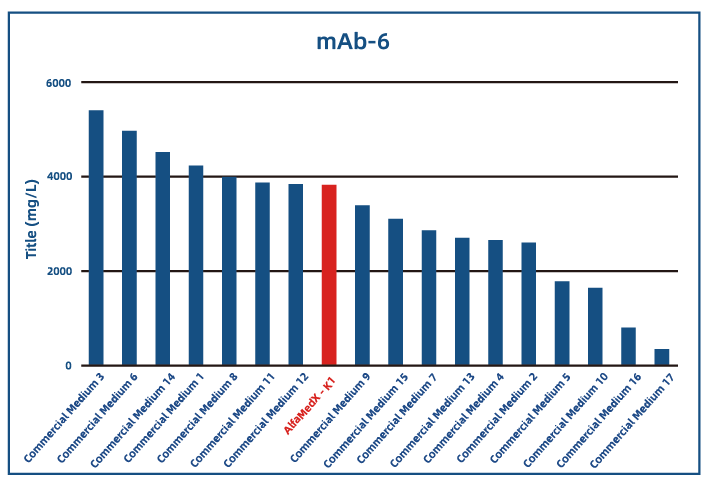
● 双抗应用
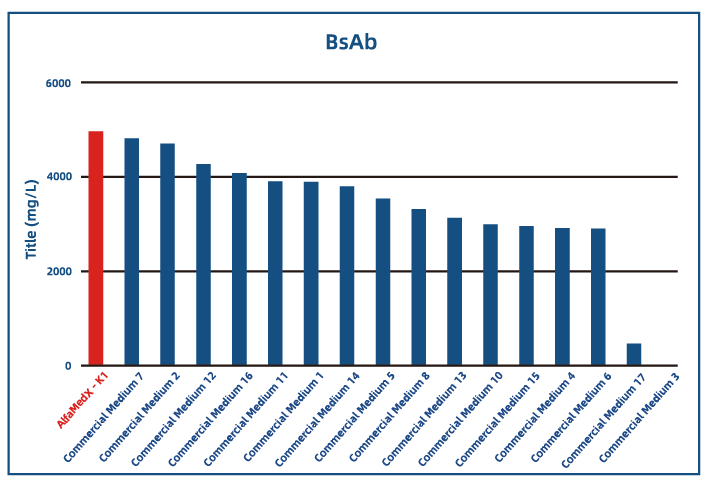
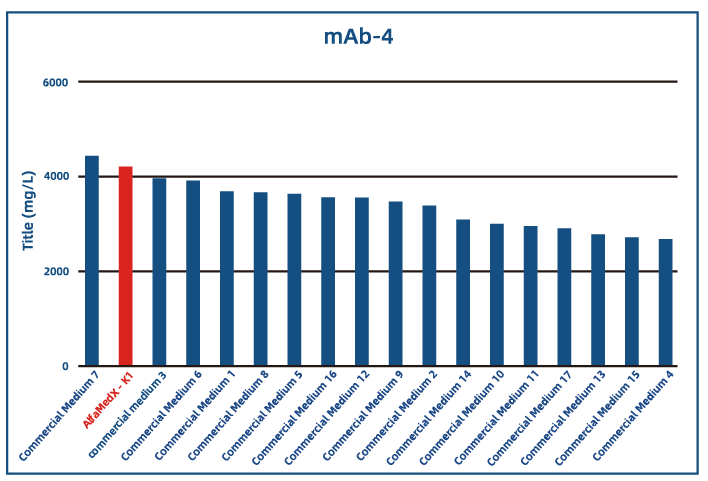
● 融合蛋白应用
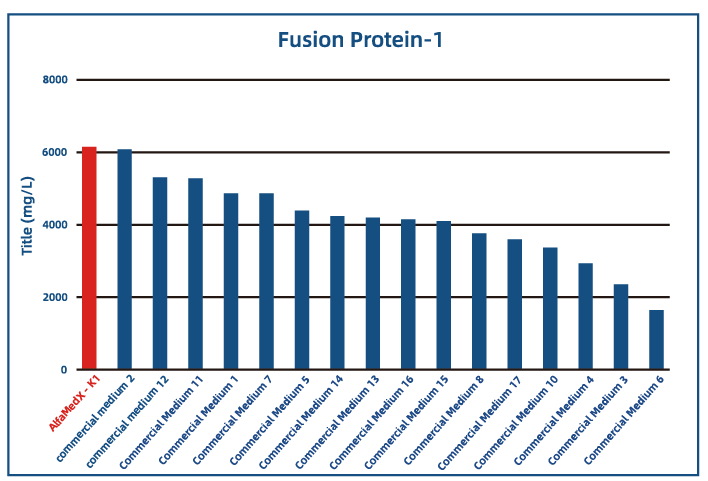
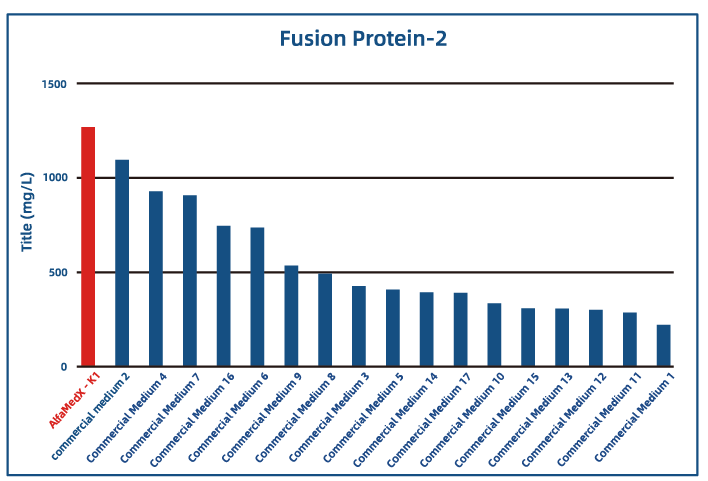
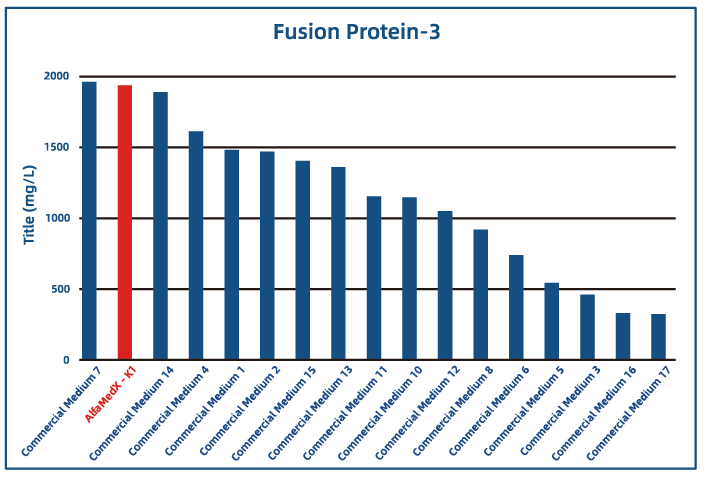
聚焦CHO-K1细胞株产品(不添加生长因子):
● 表达性能优异:蛋白表达水平与国际主流商业培养基持平,部分关键指标实现突破超越,助力提升生物药生产效率。
● 适应性广:适配多种生物药产品类型的细胞培养,覆盖融合蛋白、单抗、双抗等领域,具备广泛的产业应用潜力。
为更快地提升行业内单抗、双抗、融合蛋白等产品蛋白表达水平,AlfaMedX K1目录培养基现开放免费试用活动,欢迎在文末预约商务洽谈,携手合作、共促行业发展!
关于DMF备案
药品主文件(Drug Master Files, DMF)是持有者递交给FDA的药物存档文件,包含药物产品在生产、操作、包装和储存过程中用到的设施、操作流程、原料等保密细节信息。FDA建立了DMF体系,原料供应商以DMF文件的形式将所需的技术内容直接交给FDA备案并获得备案编号,药物申报者可以直接使用DMF备案编号来代替申报过程中需要提供有关原料和辅料的具体信息,极大程度上缩短了审查和评估时间。
邮箱:BD@greatbay-bio.com
电话:18926497707(微信同号)










